Rev Cubana Plant Med. 2016;21(3)
ARTÍCULO ORIGINAL
Optimización de las variables de extracción de flavonoides a partir de hojas de Annona muricata L.
Optimization of variables for extraction of flavonoids from Annona muricata L. leaves
Yaima Henry García,I Suslebys Salomón Izquierdo,II Jhoany Acosta Esquijarrosa,III Aylema Romero Díaz,II Marilín LópezII; Josué Mercado VidalI
I Grupo
Empresarial LABIOFAM. La Habana, Cuba.
II Centro de Investigación y Desarrollo de Medicamentos (CIDEM).
La Habana, Cuba.
III
Centro de Ingeniería de Procesos (CIPRO). Instituto Superior Politécnico
José A. Echevarría. La Habana, Cuba.
RESUMEN
Introducción:
la Annona muricata L. (guanábana) se emplea en la etnomedicina para
el tratamiento de diferentes enfermedades. Se han determinado la presencia de
flavonoides en las hojas, los cuales poseen propiedades antidiabéticas,
antioxidantes y antiinflamatorias.
Objetivo:
evaluar la influencia de parámetros operacionales de extracción en
la obtención de flavonoides a partir de las hojas de A. muricata.
Métodos:
se emplearon hojas secas, previamente molidas como material vegetal y etanol
como disolvente. La evaluación de las variables de operación se realizó
a partir de un diseño experimental de superficie respuesta compuesto central
rotacional 23 con puntos estrellas, seleccionándose los intervalos
entre 50 y 70 mL/g para la relación material vegetal-volumen de disolvente,
entre 40 y 80 % la concentración de etanol y entre 2 y 3 h el tiempo de
extracción. Se determinó la presencia de flavonoides y quercetina
en los extractos obtenidos. La cuantificación de flavonoides totales se
realizó por un método colorimétrico a 430 nm, expresado como
quercetina. Para la mejor condición experimental se realizaron experimentos
por triplicado y se comparó con el valor predicho por el diseño encontrándose
una buena correlación entre ambos.
Resultados:
la condición óptima en la extracción de flavonoides totales se
obtuvo a una concentración de etanol de un 96 %, una relación de 70
mL/g y un tiempo de 1,6 h. Las variables significativas resultaron los efectos
cuadráticos de la relación material vegetal-volumen de disolvente
y la concentración de etanol.
Conclusiones:
se seleccionaron las mejores condiciones de extracción en la obtención
de un extracto a partir de hojas de guanábana con presencia de flavonoides,
a partir de las cuales se alcanzó un rendimiento del proceso de extracción
de 87%.
Palabras clave: Annona muricata L.; flavonoides; extracción sólido-líquido.
ABSTRACT
Introduction:
Annona muricata L. (soursop) is used in ethnomedicine for the treatment
of various diseases. Leaves of this species have been found to contain flavonoids,
which are compounds with antidiabetic, antioxidant and anti-inflammatory properties.
Objective:
evaluate the influence of operational parameters on the extraction of flavonoids
from A. muricata leaves.
Methods: dry ground leaves were used as plant material and ethanol as
solvent. Evaluation of the operational variables was based on a 23
experimental rotatable response surface central composite design with star points,
selecting the intervals between 50 and 70 mL/g for the plant material / solvent
volume ratio, 40% to 80% for ethanol concentration and 2 to 3 h for extraction
time. Flavonoids and quercetin were found in the extracts obtained. Total flavonoids
were quantified using a colorimetric method at 430 nm, expressed as quercetin.
Experiments were conducted in triplicate to determine the best experimental
condition. Comparison with the design value predicted showed a good correlation
between the two.
Results: the optimal condition for extraction of total flavonoids was
reached at an ethanol concentration of 96%, a 70 mL/g ratio and a time of 1.6
h. The variables found to be significant were the quadratic effects of the plant
material / solvent volume ratio and ethanol concentration.
Conclusions: a selection was made of the best conditions to obtain an
extract from soursop leaves containing flavonoids, in which an extraction output
of 87% was achieved in the extraction process.
Key words: Annona muricata L.; flavonoids; solid-liquid extraction.
INTRODUCCIÓN
Las plantas medicinales representan el 25 % del total de las prescripciones médicas en los países industrializados; en los países en desarrollo su uso representa el 80 % del arsenal terapéutico. Debido a esto, las grandes transnacionales tienen como objetivo primordial la búsqueda de nuevas fuentes de origen vegetal y tienen en cuenta la amplia riqueza biótica presente en el planeta, donde existen aún regiones sin explorar.1,2
La Annona muricata L. también popularmente conocida como guanábana es un pequeño árbol perteneciente a la familia Annonaceae, género Annona. Es una planta de fruto comestible y se destaca por su aromática, subácida y jugosa pulpa.3 Es un árbol nativo de América Tropical, se le encuentra en todo el continente americano y se cree que su origen es la cuenca del Río Amazonas.4
Se han identificado en las hojas diferentes compuestos con actividad antiparasitaria, antipirética, antiinflamatoria, antihipertensiva, antioxidante, antidiabética, anticancerígena, analgésica y antiviral.5
Los flavonoides son metabolitos secundarios que se encuentran en todas las partes de las plantas, y cumplen una función protectora de ella y sus frutos. Así como estos compuestos tienen una función relevante en la planta, también cobran importancia farmacéutica.
Se ha identificado en extractos etanólicos de hojas de A. muricata la presencia de flavonoides, a los cuales se les atribuyen actividades farmacológicas tales como: antidiabética, antiinflamatoria y antioxidante.6,7
En LABIOFAM existe el interés de obtener un extracto rico en flavonoides debido a las diferentes propiedades que se le atribuye. Si bien aparecen diferentes reportes de extractos totales de A. muricata que refieren la presencia de flavonoides, se hace necesario la concepción de un procedimiento nacional que permita la obtención de un extracto rico en flavonoides el cual podrá ser reproducido a escala industrial para garantizar la futura demanda de este fitomedicamento.
El objetivo de este trabajo es evaluar la influencia de parámetros operacionales de extracción en la obtención de flavonoides a partir de las hojas de A. muricata.
MÉTODOS
Material vegetal
En los ensayos se utilizó hojas secas de A. muricata recolectadas de forma manual entre los meses de marzo y mayo de 2013 en el Grupo Empresarial LABIOFAM. Las hojas previamente molidas (3-5 mm de tamaño de partículas) en un molino de cuchillas modelo CEMOTEC 1090 se secaron en estufa eléctrica con recirculación de aire a 38 °C, durante un tiempo de 72 h.
Materiales
El disolvente etanol se suministró por el Grupo Empresarial LABIOFAM con una pureza del 96 %, por lo que no fue necesario someterlo a ningún proceso de purificación. El agua desionizada empleada se suministró por el Centro de Investigación y Desarrollo de Medicamentos (CIDEM).
Estudio preliminar de la influencia de los parámetros de operación en la etapa de extracción de flavonoides a partir de las hojas de A. muricata
Estudio de la influencia del disolvente en la extracción de flavonoides
Para seleccionar el tipo de disolvente se empleó 2 g de hojas y una relación volumen de disolvente-material vegetal de 50 mL/g para evitar la saturación del disolvente. El tiempo de extracción fue de 1 h. Se evaluaron diferentes concentraciones de etanol (96 %, 80 %, 60 %, 40 %, 20 %) y agua. Todos los estudios se realizaron por duplicado.
Estudio de la influencia de la relación disolvente- material vegetal en la extracción de flavonoides
Para el estudio de la influencia de la relación disolvente- material vegetal se empleó 2 g de hojas utilizándose como disolvente etanol al 80 % y un tiempo de extracción de 1 h. Las relaciones empleadas fueron de 20, 30, 40, 50, 60, 70 ml/g. Todos los estudios se realizaron por duplicado.
Estudio de la influencia del tiempo en la extracción de flavonoides
Para el estudio de la influencia del tiempo de extracción se utilizaron 6 g de material vegetal, una relación volumen de disolvente/ material vegetal de 50 mL/g y se tomaron alícuotas no representativas del líquido de extracción (4 ml) a las 0,5; 1; 1,5; 2; 2,5 y 3 h. Se empleó como disolvente etanol al 80 %. Todos los estudios se realizaron por duplicado.
Optimización de la etapa de extracción en la obtención de flavonoides a partir de hojas de A. muricata
La influencia de los parámetros de operación de la etapa de extracción: tiempo (h), relación volumen de disolvente-material vegetal (mL/g) y concentración de disolvente (%) se realizó a partir de un diseño factorial de superficie de respuesta compuesto central rotacional (23) de 17 corridas, incluyendo 6 puntos estrellas. Los niveles estudiados fueron seleccionados teniendo en cuenta los resultados preliminares obtenidos.
En cada ensayo se utilizaron 2 g de material vegetal, posterior al proceso extractivo se separó el extracto del residuo vegetal mediante gasa y se filtró bajo presión reducida, a través de lona filtrante. Como variable de respuesta se evaluó la concentración de flavonoides.
Cuantificación del contenido de flavonoides presente en las hojas de A. muricata
La determinación se realizó empleando un método colorimétrico por reacción con cloruro de aluminio en metanol, con un espectrofotómetro, a 430 nm expresados como quercetina a partir de una curva de calibración.8
Análisis estadístico
A los resultados del diseño se les realizó un análisis de varianza (ANOVA) para determinar las variables con diferencias estadísticamente significativas entre los tratamientos. Además se realizó un análisis de regresión múltiple para determinar a partir del coeficiente de determinación (R 2) y del coeficiente de determinación ajustado (Adj. R2) si existe buena correlación entre los valores obtenidos.
RESULTADOS
Estudio preliminar de la influencia de los parámetros de operación en la extracción de flavonoides a partir de las hojas de A. muricata
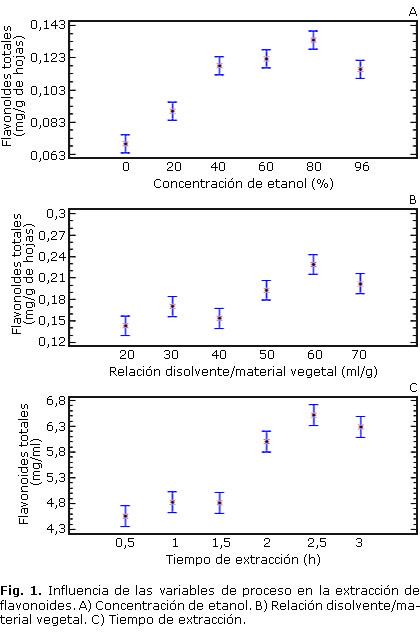
Como se aprecia en la fig 1, con el aumento de la concentración de etanol se incrementa el contenido de flavonoides, obteniéndose los mayores valores para una concentración de etanol de un 80 %.
Los valores de contenido de flavonoides extraídos fueron superiores para valores de concentraciones de etanol entre 40 y 96 %, no existiendo diferencias significativas, por lo que se decide tomar como intervalo de trabajo para el diseño entre 40 y 80 %.
Se aprecia además, que a un aumento de la relación disolvente/material vegetal se favorece la extracción de flavonoides sobre todo en el intervalo de 50 ml/g a 70 mL/g, obteniéndose un máximo a una relación de 60 mL/g. En el caso de la relación 70 mL/g se observa que ha disminuido con respecto a 60 mL/g lo cual se puede atribuir a que las hojas se hayan saturado con el disolvente por lo cual hay una disminución de la solubilidad y con ello del intercambio de soluto. Por lo anterior se decide trabajar en el intervalo de 50 mL/g a 70 mL/g en la optimización de esta variable.
Como se puede apreciar en la fig 1C, un aumento del tiempo favorece la extracción de flavonoides, obteniéndose un máximo a los 2,5 h. A las 3 h se observa una ligera disminución, lo cual se puede atribuir a una posible degradación de metabolitos.
Como se observa, existen diferencias estadísticamente significativas entre las medias de los contenidos de flavonoides totales para valores de tiempo menores de 1,5 h y mayores de este valor hasta las 3 h. Se aprecia además que al transcurrir las 3 h hay una ligera disminución en el contenido de flavonoides.
Teniendo en cuenta el comportamiento observado, se decide trabajar en el intervalo de 2 a 3 h en los estudios de optimización. (tabla 1)
Optimización de la etapa de extracción sólido-líquido en la obtención de flavonoides a partir de hojas de A. muricata
El mayor valor de concentración de flavonoides (0,205 mg/g mat.veg) se alcanzó trabajando a una concentración de etanol de 96 %, un tiempo de 2,5 h y una relación disolvente/ material vegetal de 60 mL/g y el menor valor de concentración de flavonoides se obtuvo para una concentración de etanol de 40 %, un tiempo de 3 h y una relación disolvente/ material vegetal de 50 mLl/g.
A partir de los resultados se realizó un análisis de varianza, los que se muestran en la tabla 2.
Teniendo en cuenta el análisis de varianzas se observa que las variables significativas fueron la interacción cuadrática de la relación disolvente/ material vegetal y la concentración de etanol para valores de probabilidad menores que 0,05.
Mediante la aplicación del análisis de regresión múltiple a los datos experimentales, las variables respuestas y las variables independientes se correlacionan a un polinomio de segundo orden como en la siguiente ecuación:
El análisis de variancia (ANOVA) del modelo de regresión cuadrático muestra que los valores del coeficiente de determinación (R 2) y del coeficiente de determinación ajustado (Adj. R2) fueron 85 y 76 % respectivamente, lo que sugiere un alto grado de correlación entre los valores observados y predichos.
Al analizar el diagrama de Pareto (Fig 2), se observa que el parámetro que más influye positivamente en el proceso de extracción es la influencia de la concentración de etanol, pues a mayor concentración mayor será la extracción de flavonoides. En segundo lugar influyen de forma negativa en el proceso, los efectos cuadráticos de la relación disolvente/ material vegetal.
A partir de los resultados, el gráfico de superficie de respuesta (fig 3) muestra que las condiciones más favorables para la extracción de flavonoides a partir de hojas de A. muricata bajo las condiciones evaluadas son: tiempo de extracción 1,6 h; relación disolvente/material vegetal de 62 mg/g mat. veg. y una concentración de etanol de 96 %.
DISCUSIÓN
Estudio preliminar de la influencia de los parámetros de operación en la extracción de flavonoides a partir de las hojas de A. muricata
En cuanto al comportamiento de etanol se encontraron en la literatura resultados similares al arrojado en el presente estudio.9
El comportamiento obtenido para las concentraciones de etanol y relaciones disolvente/material vegetal empleadas es esperado debido a que los procesos de extracción son más eficientes cuando la cantidad de disolvente es elevada. Generalmente grandes cantidades de disolvente pueden disolver constituyentes más eficientemente, conduciendo a un aumento del rendimiento de extracción.10 Por el contrario, pequeñas relaciones de disolvente material vegetal pueden propiciar bajos rendimientos de extracción debido a que se alcanza el equilibrio11 y al no existir una diferencia de concentración del metabolito en la fase líquida y dentro de la matriz vegetal finaliza el proceso de transferencia de masa. Por consiguiente, la elección de volúmenes apropiados de disolventes es una tarea muy importante.
En el caso de la variable tiempo el comportamiento coincide con lo reportado en la literatura en la que obtiene las mejores concentraciones de flavonoides a las 2 h de extracción.12
En este trabajo se llevó a cabo la evaluación de la influencia de los parámetros de proceso para la obtención de un extracto con presencia de flavonoides a partir de hojas de A. muricata. La concentración de la mezcla hidroalcohólica utilizada como disolvente de extracción fue el parámetro que tuvo mayor influencia en el rendimiento del proceso. Se determinaron las mejores condiciones que favorecen el proceso de extracción de flavonoides a nivel de laboratorio, utilizándose como parámetros de operación una temperatura de 50 ºC, un tiempo de 1,6 h y una relación volumen de disolvente/ material vegetal de 62 mL/g.
REFERENCIAS BIBLIOGRÁFICAS
1 Sharapin NE. Fundamentos de tecnología de productos fitoterapéuticos. In: Pinzón R, editor. Santa Fe de Bogotá, D.C., Colombia. 2000; p. 27-60.
2 Vinatoru M. An overview of the ultrasonically assisted extraction of bioactive principles from herbs. Ultrasonics Sonochemistry. 2001;(8):303-13.
3 Loc O, Cabello I, Doroteo V. (2006, Diciembre 1). Análisis de flavonoides en plantas. [citado 22 nov 2013] Disponible en: http://old.iupac.org/publications/cd/ medicinal_chemistry/Practica-VI-6.pdf .
4 Amaya J, Roldan H. Algunos aspectos sobre el cultivo de la guanábana (Annona muricata L.) Gedisa. Brasil-Brasilia. 1990; pp 6-11.
5 Gajalakshmi S, Vijayalakshmi D, Rajeswari V. Phytochemical and pharmacological properties of Annona muricata: A review. International Journal of Pharmaceutical Sciences. 2012; ISSN-0975-1491 Vol 4.
6 Gaitén G y Yamilet I. Estudio farmacognóstico de Phyllanthus orbicularis HBK, especie endémica de Cuba. Doctor en Ciencias de una Especialidad, Universidad de La Habana. 2012.
7 Foong Ch, Abdul R. Evaluation of anti-infl ammatory activities of ethanolic extract of Annona muricata leaves. Brazilian Journal of Pharmacognosy. 2012;22(6):1301-07.
8 Ochoa A, Marín J, Rivero D. Caracterización física y química de extractos totales de Petiveria alliacea L con acción antimicrobiana. Universidad de Oriente. Facultad de Ciencias Naturales. Departamento de Farmacia. 2006.
9 Victório C, Lage C, Kuster R. "Flavonoid extraction from Alpinia zerumbet (Pers.) Burtt et Smith leaves using different techniques and solvents. Eclética Química, São Paulo. 2009;34(1):19-24.
10 Li H. Application of ultrasonic technique for extracting chlorogenic acid from Eucommia ulmodies Oliv. (E. ulmodies). Ultrason Sonochem. 2005;12:295-300.
11 Valachovic P. Towards the industrial production of medicinal tincture by ultrasound assisted extraction. Ultrason Sonochem. 2001;8(2):111-7.
12 Sathishkumar T, Baskar R, Shanmungan S, Rajasekaran P, Sadasivan S, Manikandan V. Optimization of flavonoids extraction from the leaves of Tabernaemontana heyneana Wall. using L16 Orthogonal design. Nature and Science. 2008;6(3), ISSN:1545-0740.
Enviado: 12 de
junio de 2015.
Aprobado:
18 de marzo de 2016.
Yaima Henry García. Grupo de Investigación y Desarrollo. Grupo Empresarial LABIOFAM. La Habana, Cuba. Correo electrónico: yaima.henry@nauta.cu